Actualités
EFFET DE LA PRÉDATION DU LYNX BORÉAL SUR LES POPULATIONS DE CHEVREUILS EUROPÉENS DANS LE MASSIF JURASSIEN : L'IMPORTANCE DE CONSIDÉRER LES ÉCHELLES SPATIO-TEMPORELLES
Lors de la publication de la lettre Lynx boréal N°24 de la SFEPM, en décembre 2025, un article traitait de l’effet du Lynx boréal sur les populations de Chevreuils européens au sein du massif jurassien.
Afin, d’approfondir la question, voici quelques éléments d’analyse supplémentaires.
À large échelle, les effets du climat et de la chasse (anthropique) sont les principaux moteurs de la dynamique de population de chevreuils
|
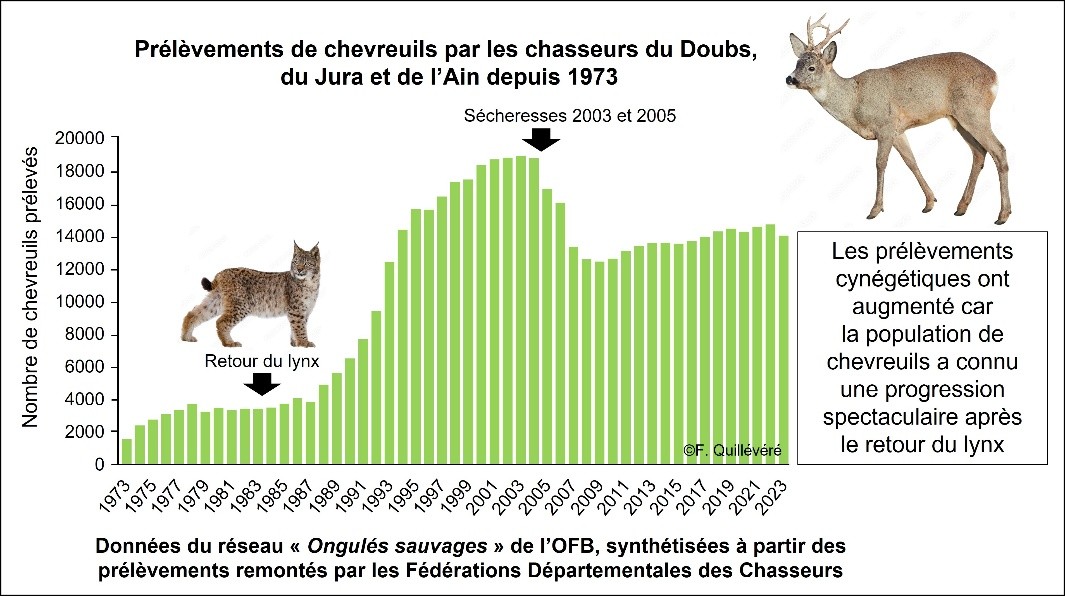
Dans cet article, l’auteur met en avant que les prélèvements (par la chasse) de chevreuils, et donc par corrélation, ses effectifs, n’ont pas diminué depuis le retour du lynx dans le massif jurassien. A l’inverse, il montre qu’ils ont augmenté jusqu’aux années 2000, dates des premières sécheresses estivales (Figure 1).
Cela montrerait que le chevreuil est bien plus impacté par le réchauffement climatique que par le félin à l’échelle du massif jurassien. En effet, nous ne pouvons qu’être d’accord sur le fait qu’à ces échelles d’analyses (interdépartementales), les principaux facteurs influençant la dynamique des populations de chevreuils sont le climat et la chasse.
Les populations de chevreuils de la Réserve Biologique Intégrale de Chizé (Deux-Sèvres) et du territoire d’étude de Trois-Fontaines (Marne), toutes deux sans grand prédateur, ont vu leur taux d’accroissement baisser de 12 et 8 % entre 1980 et 2010. La principale cause serait l’effet du réchauffement climatique sur la survie juvénile (Gaillard et al., 2013; Klein et al., 2014).
En réponse aux dérèglements climatiques, les chevrettes semblent avancer légèrement leurs dates de mises-bas de façon variable en Europe (0.06-0.33 jours/an Allemagne Hagen et al., 2021 ; 0.05 jours/an - France Plard et al., 2014 ; 0.06 jours/an - Suisse Rehnus et al., 2020). Chaque année le pic de végétation avance et accroit de plus en plus l’écart avec le pic des naissances écarte croissant de 0.54 jours/an - France Klein et al., 2014 ; Dates de naissances avancent 7.5 fois plus lentement que le début de la croissance de la végétation Suisse Rehnus et al., 2020). Ainsi, sous l’effet de l’appauvrissement de la qualité nutritive du lait, la survie des faons et la dynamique des populations sont affectées.
Les massifs de montagne étant vraisemblablement plus fortement soumis aux effets du changement climatique, il est donc largement probable que ce facteur, associé à un phénomène de densité-dépendance, ait influencé fortement la dynamique des populations de chevreuils dans le massif jurassien. Comprendre ces mécanismes est d’ailleurs l’un des objectifs d’ECOLEMM. |
Figure 1: Évolution des prélèvements à la chasse de chevreuils - Réalisé par Frédéric QUILLÉVÉRÉ, Lettre Lynx boréal N°24 SFEPM, Décembre 2025 |
À des échelles plus fines, peut-on réellement exclure l’effet de la prédation du lynx ?
Pour autant, il existe des questions d’échelles spatiales et temporelles d’analyse qui masquent d’éventuels effets de la prédation du lynx et de ses interactions avec les autres causes de perturbation (climat, chasse, maladies).
1. Évolution de l’aire de présence du Lynx boréal : une dynamique de colonisation ne permettant pas d’analyser l’effet de la prédation
|
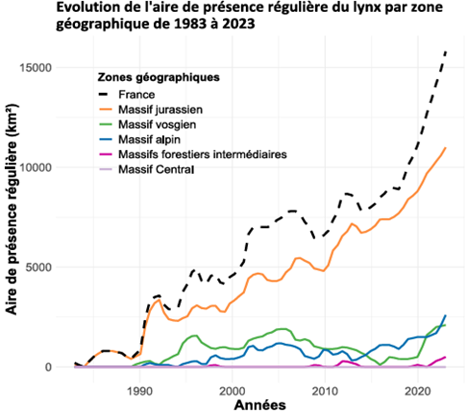
Figure 2: Évolution de l'aire de présence française du Lynx boréal |
La Figure 2 ci-contre montre que l’aire de présence jurassienne du lynx ne cesse de croitre sur la période de comparaison des plans de chasse chevreuils (JEAN et al., 2024 & Figure 1).
Cette colonisation du lynx dans le Jura s’est faite de l’Est vers l’Ouest et des altitudes « élevées » (supérieures à 1000 m) vers la plaine. Les populations de chevreuils des trois départements n’ont donc jamais, et ne sont toujours pas, soumises à une « pression de prédation par le lynx » homogène.
Nous imaginons facilement qu’un lynx sur le front de colonisation n’a pas le même effet sur la population de chevreuils que plusieurs lynx en aire de présence permanente avec des femelles régulièrement suitées.
En conclusion, à l’échelle de trois départements, il n’est actuellement pas possible de constater un effet du retour du lynx sur les populations de chevreuils.
Par ailleurs, nous ne nous attendons pas à une relation linéaire entre les effectifs du prédateur (lynx) et du chevreuil dans cette relation et ces écosystèmes anthropisés, notamment du fait de l’existence de proies secondaires : le chamois est également répandu dans le massif jurassien. L’existence de proies alternatives (chamois, lièvres, renards, etc.) représente une part non négligeable du régime alimentaire du félin (Jobin et al., 2000; Molinari-Jobin et al., 2002, 2007). De plus, il a été démontré que dans des écosystèmes anthropisés, les effets de l’humain complexifient largement les mécanismes en jeu et les réponses numériques de la proie (Kuijper et al., 2016). |
2. Évolution des prélèvements de chevreuils : une situation contrastée au sein et hors de l’aire de présence du lynx
|
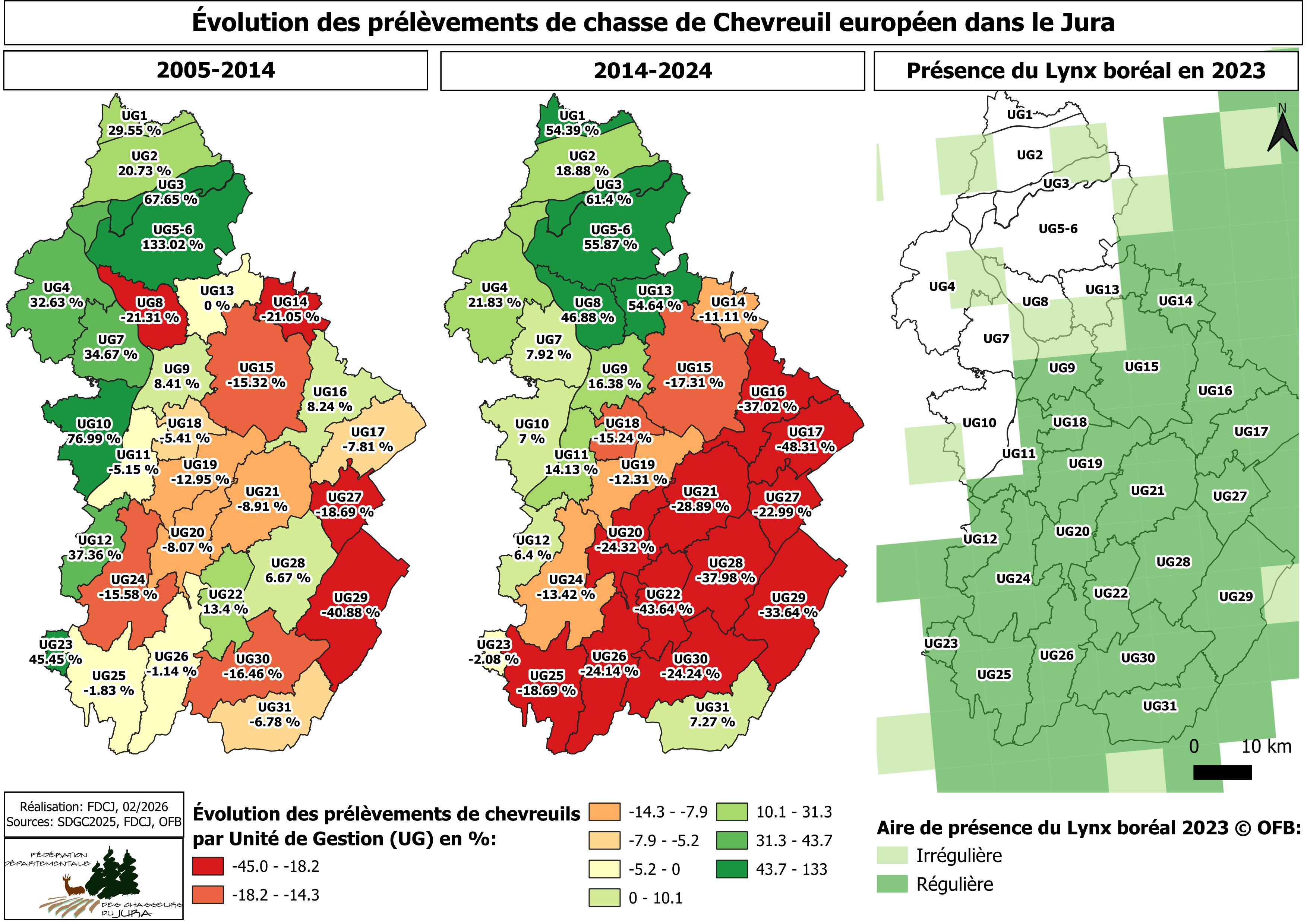
Pour ce qui est des prélèvements de chasse de chevreuils, les dynamiques départementales lissent des dynamiques locales beaucoup plus contrastées (Figure 3).
À titre d’exemple pour le département du Jura, nous constatons deux situations :
La hausse des prélèvements, surtout marquée dès 2010, dans le bas Jura a donc masqué/compensé la baisse dès le premier plateau, surtout marquée dès 2010. Cela illustre bien comment les analyses à des échelles départementales peuvent limiter les dynamiques plus locales et leurs perceptions.
De plus, en considérant que les prélèvements de chasse seraient largement corrélés à la densité de chevreuils, nous pourrions conclure que la présence du lynx (Figure 3) a un effet significatif sur les populations de cet ongulé dans le Jura et aurait réduit de 22.7% la population en 10 ans au sein de son aire de présence.
Or, la prise de recul nous conduit à relativiser cette conclusion pour plusieurs raisons :
|
Figure 3: Évolution des prélèvements de chevreuils par la chasse dans le Jura, entre 2005 (date minimum de disposition des données par Unités de Gestion) et 2024 – Surface moyenne des UG : 168 km² |
Ainsi, considérant les chiffres exposés, écarter un effet de la prédation du lynx sur les populations de chevreuils à l’échelle départementale serait abusif, de même que considérer qu’elle en est le seul facteur explicatif à l’échelle des unités de gestion.
Que dit la littérature scientifique ? Un effet de la prédation du lynx incontestable, mais dépendant de divers facteurs.
Changeons une nouvelle fois d’échelle pour s’intéresser à ce que conclut la littérature scientifique européenne.
Une synthèse d’études sur les facteurs explicatifs des densités de chevreuils en Europe a montré que celles-ci étaient largement expliquées par la productivité de la végétation, la couverture forestière et l’absence ou présence de lynx et de loup (Melis et al., 2009). La densité de chevreuils est largement plus faible en présence de prédateurs et cela est d’autant plus vrai lorsque loup et lynx sont présents ensemble. De plus, moins les écosystèmes sont productifs (en termes de végétation), plus la prédation aurait un effet sur la densité de chevreuils. Par ailleurs, le chevreuil est une espèce dont la survie peut être impactée par une forte sévérité hivernale (Gaillard et al., 1993; Okarma et al., 1995). Aussi, en présence de prédateurs, dont le Lynx boréal, la hauteur de neige réduisant la mobilité des chevreuils, pourrait accentuer la prédation du félin (Melis et al., 2009).
La pose de colliers GPS/VHF sur des chevreuils au sein du Parc National de Bavière en Allemagne, avant et après le retour du lynx, a permis de conclure à une baisse du taux de survie de 0.79 à 0.61 (Heurich et al., 2012). En Suède, le taux de croissance d’une population de chevreuils serait affecté de 11 % (Andrén & Liberg, 2015) par la prédation du félin à la suite de son retour sur la zone d’étude. La proportion de la prédation du lynx varie selon les études, a entre 2005 et 2008 (Heurich et al., 2012), 12 % des causes de mortalités de l’ongulé entre 1983 et 1985 dans les Alpes Suisses (Breitenmoser & Haller, 1987), puis 62% dans cette même région entre 1997 et 2011 (BREITENMOSER & Breitenmoser-Würsten, 2008), 30 % dans le Jura Suisse entre 1988 et 1998 (Molinari-Jobin et al., 2002), 39 % en Pologne entre 1991 et 1996 (Okarma et al., 1997). Molinari-Jobin et al., 2002 mettent en avant dans le Jura Suisse, le fait que la prédation du lynx concernerait respectivement un maximum de 9 % et 11 % de la population printanière de chevreuil et de chamois.
Ces études illustrent la variation des effets du lynx sur le chevreuil, notamment dépendante des conditions initiales de la population et de sa densité. En effet, plus les densités initiales de chevreuils sont faibles, en lien avec la productivité des écosystèmes, plus la part de la prédation est forte (Melis et al., 2007; Nilsen et al., 2009). Andrén & Liberg, 2023 ont même mis en avant des relations cycliques entre les densités de lynx et les densités de chevreuils, uniquement observées dans des régions peu productives de la Suède.
Cependant, Kuijper et al., 2016 mettent en avant qu’au sein d’écosystèmes anthropisés, comme en Europe occidentale, l’effet des grands-prédateurs dépendrait du contexte et, qu’à l’exception des écosystèmes peu productifs, l’effet des activités humaines serait supérieur à celui des prédateurs.
Ainsi, en influençant les densités de chevreuils, les politiques de gestion par la chasse sont susceptibles d’affecter indirectement l’effet de la prédation. Il en est de même de la compétition interspécifique avec le Cerf élaphe (Borkowski et al., 2021; Franchini et al., 2023) ou de la prédation des faons par les sangliers en fortes densités (MELBERG, 2012) et le pâturage d’animaux domestiques (Horcajada-Sánchez et al., 2019).
Parmi les mécanismes en jeu, la question d’une prédation additive ou compensatoire des autres causes de mortalité est intéressante, car elle peut changer la nature de la réponse numérique de la proie. Pour les chamois, Vogt et al., 2019 ont montré dans les Alpes suisses que la prédation du lynx était partiellement compensatoire aux autres causes de mortalités, par une prédation plus marquée sur les chevreaux et vieux individus.
Pour le chevreuil en revanche, il semblerait que de par son mode de prédation, le lynx ne sélectionne les proies les plus faibles et aurait une prédation plus aléatoire (Andersen et al., 2007; Andrén & Liberg, 2015). Cela diffère du chasseur, qui selon les modes de chasse peut sélectionner les adultes, ou alors les jeunes en fonction des stratégies de gestion De plus, Gehr et al., 2018 ont montré en Suisse que sous l’effet de la pression de chasse anthropique, les chevreuils adapteraient leur utilisation de l’habitat pour échapper aux chasseurs (principalement en milieux ouverts), les rendant plus sensibles à la prédation du lynx. Enfin, tout le champ des effets non létaux de la prédation naturelle et anthropique pourrait être exposé. Sans entrer dans les détails, Gehr, J Hofer, et al., 2018 ont montré que la survie du chevreuil était plus impactée par les comportements de vigilance déployés par cet ongulé pour éviter la prédation du lynx que pour éviter la proximité aux activités humaines.
Sans se vouloir exhaustif, ce rapide tour d’horizon des études européennes montre bien que l’effet de la prédation du lynx sur les populations de chevreuils est incontestable et dépendant de la densité de chevreuils, en lien avec la productivité du milieu, de la présence d’autres prédateurs comme le loup, de la couverture forestière, mais aussi des activités humaines en présence.
En conclusion, prudence sur les conclusions et nécessité de connaissances dans des contextes contrastés
Avec les données actuelles, il n’est pas possible de conclure à l’effet de la prédation du lynx à l’échelle de trois départements, sur la base des prélèvements de chasse. Il en va de même à l’échelle intra-départementale.
Pour avoir une vision plus réaliste de la situation dans le massif jurassien, il est nécessaire de conduire des études de la dynamique des populations, telles ECOLEMM, pour avoir une vision plus objective des effets de chaque source de mortalité sur la démographie des chevreuils. Celles-ci apporteront des connaissances supplémentaires dans le contexte du massif jurassien français, sans pour autant se vouloir transposables à toutes les situations, puisque nous l’avons vu, l’effet de la prédation est multifactoriel.
Par ailleurs, idéalement, il faudrait pouvoir identifier si la prédation est additive ou compensatoire des autres sources de mortalité, via la pose de colliers GPS sur les lynx et des recherches de proies, comparées aux tableaux de chasse et aux mortalités constatés sur des ongulés marqués.
À ce jour, et en attendant les analyses plus poussées de nos données collectées dans le cadre d’ECOLEMM, 27.8 % des causes de mortalités des chevreuils capturés, marqués et suivis dans le Jura sont liées à la prédation du lynx et 22.9 % aux prélèvements de chasse.
Finalement, l’enjeu en termes de conservation et de gestion des espèces n’est pas de remettre en question l’effet de la prédation du lynx sur le chevreuil, qui a largement été démontré avec des intensités variables en Europe. Il s’agit plutôt d’améliorer notre compréhension du fonctionnement des populations de proies sous l’effet de la prédation du lynx (mais aussi du loup), de la chasse et des autres facteurs sanitaires et environnementaux, avec un large effet du changement climatique à explorer.
Ces connaissances sont favorables à une gestion durable par la chasse des populations de proies et donc à la coexistence entre les activités humaines et la présence du Lynx boréal.
Rédaction: Jean-Baptiste FANJUL, Chargé d'études ECOLEMM FDC39/01
Relecture: OFB, KORA, SFEPM
Bibliographie:
Andersen, R., Karlsen, J., Bendik Austmo, L., Odden, J., Linnell, J., & Gaillard, J.-M. (2007). Selectivity of Eurasian lynx Lynx lynx and recreational hunters for age, sex and body condition in roe deer Capreolus capreolus. Wildlife Biology, 13, 467‑474.
Andrén, H., & Liberg, O. (2015). Large Impact of Eurasian Lynx Predation on Roe Deer Population Dynamics. 3(10). https://doi.org/10 Andrén, H., & Liberg, O. (2023). Numerical response of predator to prey : Dynamic interactions and population cycles in Eurasian lynx and roe deer. Ecological Monographs, 94. https://doi.org/10.1002/ecm.1594
Borkowski, J., Banul, R., Jurkiewicz-Azab, J., Hołdyński, C., Święczkowska, J., Nasiadko, M., & Załuski, D. (2021). There is only one winner : The negative impact of red deer density on roe deer numbers and distribution in the Słowiński National Park and its vicinity. Ecology and Evolution, 11(11), 6889‑6899. https://doi.org/10.1002/ece3.7538
Breitenmoser, U., & Breitenmoser-Würsten, C. (2008). Der Luchs. Ein Großraubtier in der Kulturlandschaft. Salm Verlag. Wohlen und Bern., (Band 2), 537.
Breitenmoser, U., & Haller, H. (1987). Zur Nahrungsökologie des Luchses Lynx lynx in den schweizerischen Nordalpen. Z. Saeugetierk, 52, 168‑191.
Franchini, M., Peric, T., Frangini, L., Prandi, A., Comin, A., Rota, M., & Filacorda, S. (2023). You’re stressing me out ! Effect of interspecific competition from red deer on roe deer physiological stress response. Journal of Zoology, 320(1), 63‑74. https://doi.org/10.1111/jzo.13058
Gaillard, J.-M., Delorme, D., Boutin, J.-M., Van Laere, G., Biosaubert, B., & Pradel, R. (1993). Roe deer survival patterns : A comparative analysis of contrasting populations. Journal of Animal Ecology, (62), 778‑791.
Gaillard, J.-M., Mark Hewison, A. J., Klein, F., Plard, F., Douhard, M., Davison, R., & Bonenfant, C. (2013). How does climate change influence demographic processes of widespread species ? Lessons from the comparative analysis of contrasted populations of roe deer. Ecology Letters, 16(s1), 48‑57. https://doi.org/10.1111/ele.12059
Gehr, B., Hofer, E. J., Pewsner, M., Ryser, A., Vimercati, E., Vogt, K., & Keller, L. F. (2018). Hunting-mediated predator facilitation and superadditive mortality in a European ungulate. Ecology and Evolution, 8(1), 109‑119. https://doi.org/10.1002/ece3.3642
Gehr, B., J Hofer, E., Ryser, A., Vimercati, E., Vogt, K., & Keller, L. (2018). Evidence for nonconsumptive effects from a large predator in an ungulate prey? 29. https://doi.org/10.1093/beheco/ary031
Hagen, R., Ortmann, S., Elliger, A., & Arnold, J. (2021). Advanced roe deer (Capreolus capreolus) parturition date in response to climate change. Ecosphere, 12(11), e03819. https://doi.org/10.1002/ecs2.3819
Heurich, M., Möst, L., Schauberger, G., Sennhenn-Reulen, H., Sustr, P., & Hothorn, T. (2012). Survival and causes of death of European Roe Deer before and after Eurasian Lynx reintroduction in the Bavarian Forest National Park. European Journal of Wildlife Research, 58(3), 567‑578. https://doi.org/10.1007/s10344-011-0606-y
Horcajada-Sánchez, F., Escribano-Ávila, G., Lara-Romero, C., Virgós, E., & Barja, I. (2019). The effect of livestock on the physiological condition of roe deer (Capreolus capreolus) is modulated by habitat quality. Scientific Reports, 9(1), 15953. https://doi.org/10.1038/s41598-019-52290-7
Jean, N., Helluy, M., Barizeau, F., Chenesseau, D., Mauron, N., Schwoerer, M.-L., & Vandel. (2024). Lynx, Flash info N°12 2024 (p. 7). Lettre d’information du Réseau Loup Lynx. https://oai-gem.ofb.fr/exl-php/document-affiche/ofb_recherche_oai/OUVRE_DOC/61781?fic=doc00085414.pdf
Jobin, A., Molinari, P., & Breitenmoser, U. (2000). Prey spectrum, prey preference and consumption rates of Eurasian lynx in the Swiss Jura Mountains. Acta Theriologica, 45, 243‑252. https://doi.org/10.4098/AT.arch.00-26 Klein, F.,
Plard, F., Warnant, C., CAPRON, Gaillard, J.-M., HEWISON, M., & BONENFANT, C. (2014). Le chevreuil face aux changements climatiques : Une adaptation impossible ? Connaissance et gestion des espèces. Faune Sauvage, (303), 29‑35.
Kuijper, D. P. J., Sahlén, E., Elmhagen, B., Chamaillé-Jammes, S., Sand, H., Lone, K., & Cromsigt, J. (2016). Paws without claws ? Ecological effects of large carnivores in anthropogenic landscapes. Proceedings of the Royal Society B: Biological Sciences, 283, 20161625. https://doi.org/10.1098/rspb.2016.1625
Melberg, S. (2012). Spatiotemporal competition patterns of Swedish roe deer and wild boar during the fawning season. [Master Thesis in Wildlife Ecology]. Swedish University of Agricultural Sciences.
Melis, C., Jędrzejewska, B., Apollonio, M., Bartoń, K., Jedrzejewski, W., Linnell, J., Kojola, I., Kusak, J., Adamič, M., Ciuti, S., Delehan, I., Dykyy, I., Krapinec, K., Mattioli, L., Sagaydak, A., Samchuk, N., Schmidt, K., Shkvyria, M., Sidorovich, V., & Zhyla, S. (2009). Predation has a greater impact in less productive environments : Variation in roe deer, Capreolus capreolus, population density across Europe. Global Ecology and Biogeography, 18, 724‑734. https://doi.org/0.1111/j.1466-8238.2009.00480.x
Melis, C., Linnell, J., Odden, J., & Andersen, R. (2007). Survival rates and causes of mortality of roe deer in a multipredator system. https://doi.org/10.13140/RG.2.2.15893.52968
Molinari-Jobin, A., Molinari, P., Breitenmoser-Würsten, C., & Breitenmoser, U. (2002). Significance of lynx Lynx lynx predation for roe deer Capreolus capreolus and chamois Rupicapra rupicapra mortality in the Swiss Jura Mountains. Wildlife Biology, 8(1), 109‑115. https://doi.org/10.2981/wlb.2002.015
Molinari-Jobin, A., Zimmermann, F., Breitenmoser, C., & Breitenmoser, U. (2007). Variation in diet, prey selectivity and home-range size of Eurasian lynx Lynx lynx in Switzerland. Wildlife Biology, 13(4), 393‑405. https://doi.org/10.2981/0909-6396
Nilsen, E., Linnell, J., Odden, J., & Andersen, R. (2009). Climate, season, and social status modulate the functional response of an efficient stalking predator : The Eurasian Lynx. The Journal of animal ecology, 78, 741‑751. https://doi.org/10.1111/j.1365-2656.2009.01547.x
Okarma, H., B, J., Jedrzejewski, W., Krasiński, Z., & L, M. (1995). The roles of predation, snow cover, acorn crop, and man-related factors on ungulate mortality in Białowieża Primeval Forest, Poland. Acta theriologica, 40, 197‑217. https://doi.org/10.4098/AT.arch.95-20
Okarma, H., JĘDRZEJEWSKI, W., SCHMIDT, K., KOWALCZYK, R., & JĘDRZEJEWSKA, B. (1997). Predation of eurasian lynx on roe deer and deer Białowieża Primeval Forest. Acta Theriologica, 42(2), 203‑224.
Plard, F., Gaillard, J.-M., Coulson, T., Hewison, A. J. M., Delorme, D., Warnant, C., & Bonenfant, C. (2014). Mismatch Between Birth Date and Vegetation Phenology Slows the Demography of Roe Deer. PLOS Biology, 12(4), 1‑8. https://doi.org/10.1371/journal.pbio.1001828
Rehnus, M., Peláez, M., & Bollmann, K. (2020). Advancing plant phenology causes an increasing trophic mismatch in an income breeder across a wide elevational range. Ecosphere, 11(6), e03144. https://doi.org/10.1002/ecs2.3144
Vogt, K., Signer, S., Ryser, A., Schaufelberger, L., Nagl, D., Breitenmoser, U., & Willisch, C. (2019). Einfluss von Luchsprädation und Jagd auf die Gämse – Teil 1 und 2. Bericht in Zusammenarbeit mit dem Jagdinspektorat des Kantons Bern. KORA Bericht Nr. 84. https://www.kora.ch/?action=get_file&id=102&resource_link_id=15c